咨询热线:400-678-7252
客诉专线:400-811-5300
全部产品分类
Triethyl orthoacetate
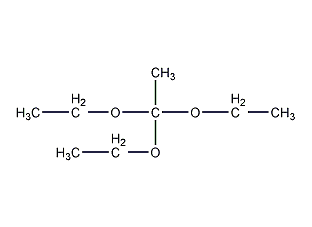
| 原乙酸三乙酯 基本信息 | |||
|---|---|---|---|
| CAS号 | 78-39-7 | 分子式 | C8H18O3 |
| 分子量 | 162 | 精确质量 | 162 |
| PSA | LogP | ||

 基础参数
基础参数
 物化性质
物化性质1. 性状:无色有特殊气味液体
2. 密度(g/mL,25/4℃):0.8847
3. 常温折射率(n20):1.3968
4. 熔点(ºC):74-78
5. 沸点(ºC,常压):144~146℃
6. 沸点(ºC,5.2kPa):47~45℃(1.60kPa)
7. 折射率:1.3949
8. 闪点(ºC):55℃
9. 比旋光度(º):不确定
10. 自燃点或引燃温度(ºC):不确定
11. 蒸气压(kPa,25ºC):不确定
12. 饱和蒸气压(kPa,60ºC):不确定
13. 燃烧热(KJ/mol):不确定
14. 临界温度(ºC):不确定
15. 临界压力(KPa):不确定
16. 油水(辛醇/水)分配系数的对数值:不确定
17. 爆炸上限(%,V/V):不确定
18. 爆炸下限(%,V/V):不确定
19. 溶解性:不溶于冷水,与乙醇、醚、酸、酯、氯仿、四氯化碳混溶。
 合成方法
合成方法
1.在无水乙腈、无水乙醇和无水乙醚的混合物中通入稍过量的干燥氯化氢制得。
2.乙酸亚胺甲基醚盐酸盐的制备 在冷却的135克无水乙睛、200毫升绝对乙醇和120毫升绝对乙醚的混合物中,通入稍超过摩尔量的千燥氯化氢。在冰箱中放置过夜后,混合物固化成为白色发光片状的块。倾去乙醚,在放有碱石灰的真空干燥器中使此盐酸盐干燥24小时,以除去过量的氯化氢。产率86-95%。 用甲醇代替乙醇进行此反应,得到白色发光片状的乙酸亚胺甲基醚盐酸盐,产率71.6%。
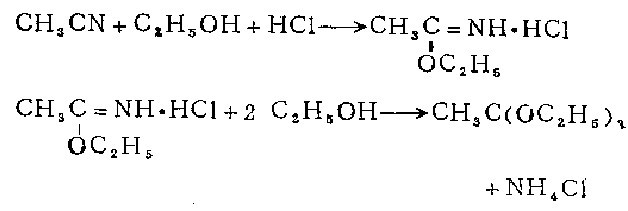
原乙酸三乙酯的制备 在350克绝对干燥而不含游离氯化氢的乙酸亚胺甲基醚盐酸盐中加入750毫升绝对乙醇。将此混合物盛于塞紧的瓶中,置千燥处放两星期,不时摇动。滤去析出的氯化按。这些氯化按要保留下来,因为乙醇与亚胺醚盐酸盐的反应极慢,故固体沉淀中还含有大量的未反应的盐酸盐。滤液用2克熔融过的碳酸钾处理以除去任何痕量的氯化氢,然后在40一60毫米的减压下分馏。第一馏分25-35℃,含绝对乙晾和一些原乙酸醋,可再用于氯化按沉淀 的和新的乙酞亚胺乙基醚盐酸盐的进一步处理。收集的沸点55-57℃/ 50mm馏分在常压下再分馏。纯原乙酸三乙醋的沸点为144-146℃而不分解。4次制备得750毫升纯产品。
 凯茵合作品牌
凯茵合作品牌
 用途&贮存
用途&贮存
1.用于反式三取代烯及手性丙二烯等烯类制剂的制备及染料、制药工业的原料。
2.原乙酸三乙酯[1]在碱性条件下稳定,酸性条件下易反应,在比较温和的条件下通过酸催化水解生成酯和醇。它水解生成乙酸乙酯和乙醇,因此这类化合物在Fischer酯化反应中会与副产物水反应,生成低沸点的乙酸乙酯和乙醇,从而使平衡移动,促进酯化反应进行。原乙酸三乙酯可以引发烯丙醇的Claisen重排,因此常用于增长碳链。此外它还可以用于合成酰胺的反应。
乙酸酯的合成 在无水条件下,一些醇也会与原乙酸三乙酯反应生成醚 (式1)[2]。一些金属配合物也可发生此类反应 (式2)[3]。
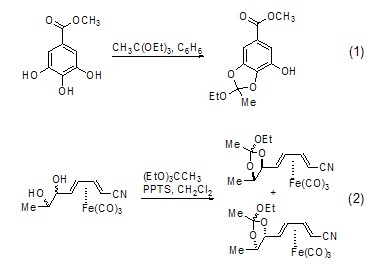
Claisen重排 在酸催化下,原乙酸三乙酯可以与烯丙醇反应生成C-C键 (式3)[4],其本质是烷氧基的Claisen重排。该反应可能生成多种手性异构体,具有一定的空间选择性 (式4)[5]。
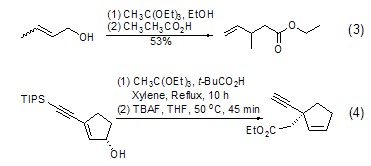
通过Claisen重排可以实现碳链的增长。由于重排产物为酯,可进一步还原为羟基,从而使碳链增长 (式5)[6]。

丙二烯的生成 原乙酸三乙酯可以与α-位取代的炔烃反应,生成具有丙二烯结构的酯 (式6)[7]。
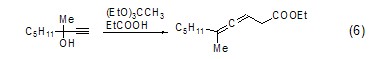
碳-碳双键的生成 原乙酸三乙酯可以作为亲核试剂进攻电子云密度较低的碳原子,形成碳-碳双键,例如它与1,3-丙二腈的反应 (式7)[8]。
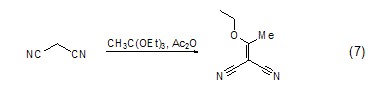
C-X键的形成 原乙酸三乙酯还可以与氨基等杂原子基团反应,形成C-N键或C=N双键 (式8)[9]。

对水敏感,需要干燥保存。
干燥保存。
 分子结构
分子结构
1、 摩尔折射率:44.31
2、 摩尔体积(cm3/mol):179.7
3、 等张比容(90.2K):404.5
4、 表面张力(dyne/cm):25.6
5、 极化率(10-24cm3):17.56
 凯茵主营品类
凯茵主营品类
 计算化学数据
计算化学数据
1.疏水参数计算参考值(XlogP):1.3
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:6
5.互变异构体数量:无
6.拓扑分子极性表面积27.7
7.重原子数量:11
8.表面电荷:0
9.复杂度:76.3
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
声明:该栏目及页面中图片、产品参数数据来源于互联网,仅供用于参考了解化学品信息,不等同凯茵化工实际销售产品。